

快速从药物活性纳米抗体
筛选推进至产业化开发

传统抗体分子量约150kDa,大小尺寸为14.2 nm × 8.2 nm × 3.8 nm,使其实体瘤的穿透性差,实体瘤的疗效不理想。来自于驼类和鲨鱼的纳米抗体(重链可变区VHH),分子量约为传统抗体的十分之一,让人们看到了实体瘤治疗的希望。本文总结纳米抗体的八个优势,以及在肿瘤诊断临床中的六个应用
1.什么是纳米抗体
骆驼体内存在天然的缺失轻链的重链抗体,克隆其可变区可以得到只有重链可变区组成的单域抗体,称为VHH(Variable domain of heavy chain of heavy chain antibody),也称为纳米抗体(Nanobody, a single domain antibody),它是最小的功能性抗原结合片段。
2.纳米抗体和普通抗体的区别
感染或者免疫过的骆驼或羊驼除了产生单克隆抗体外还会分泌一种独特的及仅有重链的抗体,这两种类型的抗体均有与抗原结合的能力。重链抗体缺少普通抗体所有的CH1区域,且CDR1和CDR3要比VH长,这在一定程度上弥补了缺失轻链造成的抗原结合力下降的不足。二者结构上差异如下图所示:


纳米抗体优势:
1)结构稳定,耐高温;纳米抗体仅有一个结构域,不含传统的连接肽序列。除了域内保守的二硫键,VHH CDR3中的CYS还可以与CDR1或FR2中的CYS形成二硫键,这些增加的序列和loop结构扩大了抗体与抗原结合的面积以及抗体的多样性,同时导致其结构非常稳定,能够耐受高温及苛刻的极端环境。
2)避免了引起的补体反应:纳米抗体没有传统的Fc段,从而避免了Fc段引起的补体反应。
3)纳米抗体易于进行基因操作。从而形成单价、双价、双特异及多价抗体,同时也能形成融合蛋白进行靶向治疗。
4)纳米抗体对人体免疫原性较弱,相容性好。比较VH germline序列及单峰骆驼germline序列,前者大约50种,后者大约40种。骆驼的VHH胚系基因序列和人类VH3家族序列高度同源,因此对VHH进行人源化比较简单。
5)纳米抗体分子量小,结构简单:由单一的基因编码,因此在噬菌体、细菌及酵母中能大量表达。
6)纳米抗体具有强而快的穿透能力,利于它们进入实体瘤中发挥作用,同时由于其能穿透血脑屏障,为脑部给药提供了新方法。
总结:和普通抗体相比,纳米抗体分子量小,结构简单,易于进行基因改造,体积小,抗原特异性好,组织穿透力强,稳定性高,在疾病的诊断及治疗方面有广阔的应用前景。
3.纳米抗体临床研究进展
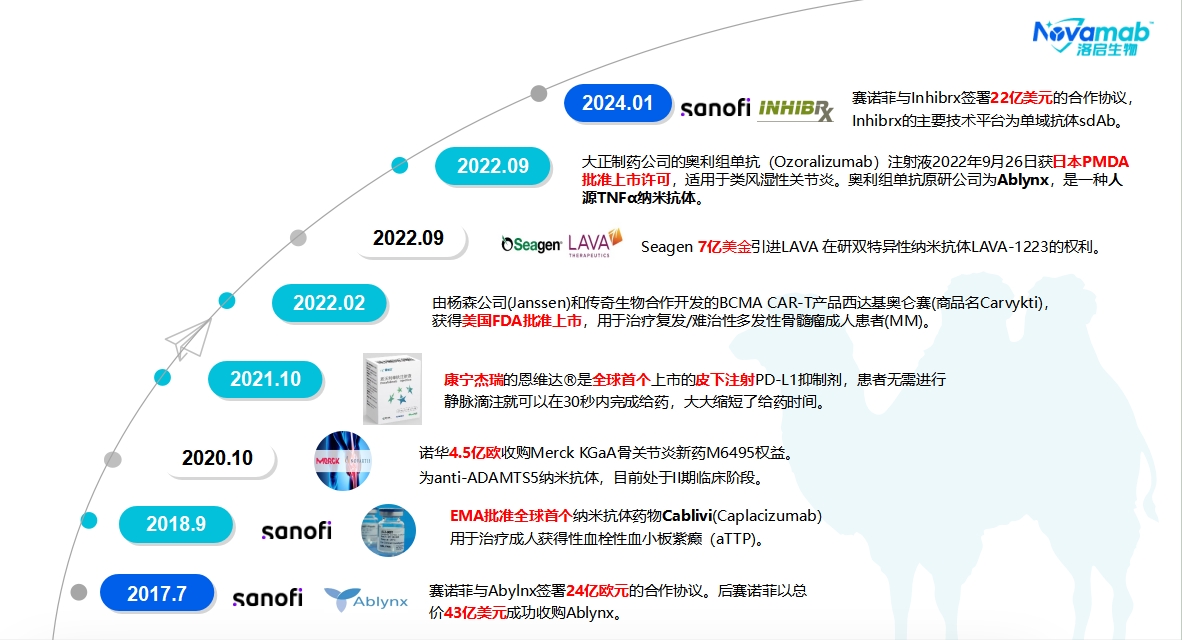
自从1993年首次发现重链抗体,其抗原结合域纳米抗体就受到了广泛关注,关于纳米抗体的研究文献与报道呈指数增加。2018年第一个纳米抗体药Cablivi(caplacizumab)于欧盟EMA批准上市,随后在FDA与加拿大卫生部批准上市,用于获得性血栓性血小板减少性紫癜(aTTP)成人患者的治疗。2021年10月,苏州康宁杰瑞的恩维达®是全球首个上市的皮下注射PD-L1抑制剂,患者无需进行静脉滴注就可以在30秒内完成给药,大大缩短了给药时间。2022年02月,由杨森公司(Janssen)和传奇生物合作开发的BCMA CAR-T产品西达基奥仑赛(商品名Carvykti),获得美国FDA批准上市,用于治疗复发/难治性多发性骨髓瘤成人患者(MM)。2022年09月,大正制药的奥利组单抗(Ozoralizumab)注射液获日本PMDA批准上市许可,适用于类风湿性关节炎。奥利组单抗原研公司为Ablynx,是一种人源TNFα纳米抗体。
此外,全球目前有多个纳米抗体药物处于不同药物研发阶段,适应症广阔,药物创新性明显,药物开发前景广阔。
![]()